
microRNA (miRNAs) 的异常表达在类风湿性关节炎 (RA) 的发病机制中起重要作用,因此基于 miRNA 的疗法已成为 RA 治疗的一种有前途的方法。在此,miR-30a 被成功筛选并确定为 RA 炎症的重要介质。MiR-30a 可直接靶向 Snai1 基因并进一步调节 Cad11 表达,抑制 NF-κB 和 MAPK 信号通路,有助于抗炎作用。为了提高 miR-30a 的治疗效果,开发了氟化聚酰胺胺树状大分子 (FP) 作为载体,以实现 miR-30a 在胶原诱导的关节炎小鼠中的递送。载体 FP 和 miR-30a 形成稳定的纳米复合物,并有效介导 miR-30a 的转染,在脂多糖刺激的巨噬细胞中执行抗炎反应。此外,FP/miR-30a 的静脉给药在发炎的关节中表现出明显的积累,并通过 Snai1/Cad11 轴抑制炎症反应,从而有助于抗关节炎疗效。此外,FP/miR-30a 纳米复合物显示出良好的生物相容性,因为它们在全身给药后不会造成器官损伤。综上所述,我们的研究表明 miR-30a 是一种有效的抗炎寡核苷酸,氟化树枝状聚合物介导的 miR-30a 递送有可能成为治疗 RA 和其他自身免疫性疾病的一种有前途的方法。
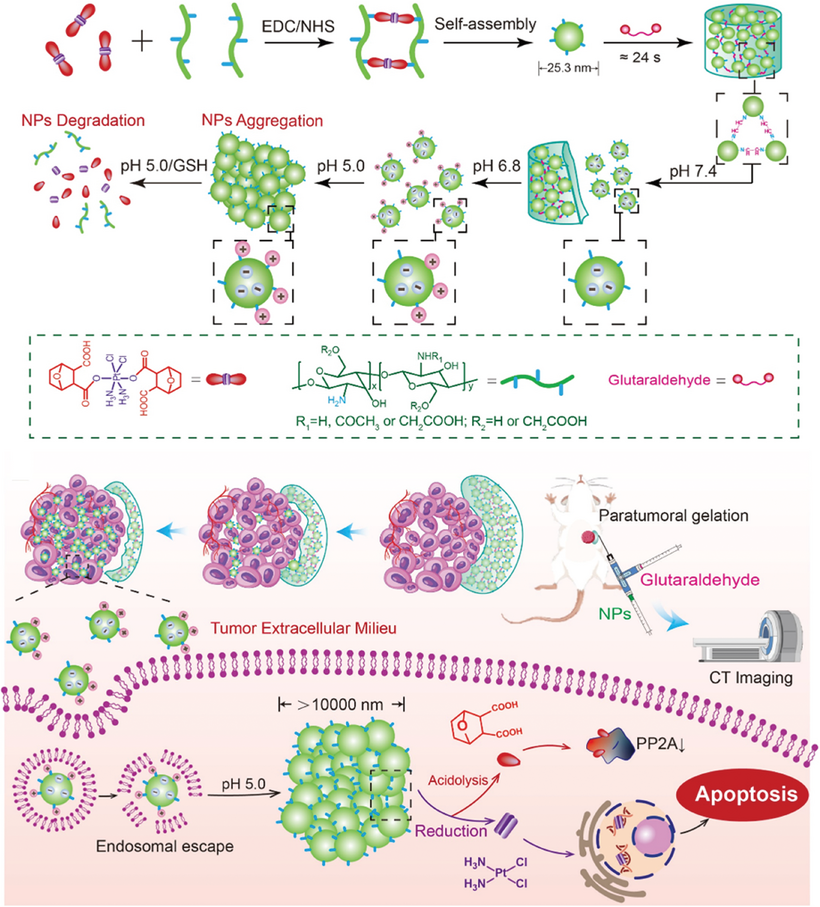
局部注射型肿瘤治疗与诊断纳米复合水凝胶由于其将两种系统的优势集成并同时最小化其缺点,展现出了巨大的临床转化潜力。然而,如何高效地让纳米药物从水凝胶中释放,并克服肿瘤渗透与积累之间的内在冲突,直接决定了其治疗与诊断效率。本文开发了一种通过席夫碱反应合成的集群导弹灵感动态纳米复合水凝胶,该水凝胶由交联的协同尺寸可变化的纳米前药(NPs)与戊二醛(GA)组成。类比集群导弹,该水凝胶能够高效释放初始尺寸为25.3 nm的纳米药物,响应肿瘤外部pH环境进行深度肿瘤分布和细胞内摄取,同时在肿瘤细胞内部pH和谷胱甘肽(GSH)的响应下,精确调控细胞内积累并高选择性地释放药物,从而实现强效的局部化化疗。此外,纳米药物中的铂重金属赋予水凝胶监测自身及肿瘤组织动态变化的能力,无需额外常规成像剂。因此,这种集群导弹灵感的动态纳米复合水凝胶为精确局部肿瘤治疗与诊断提供了新的临床应用路径。
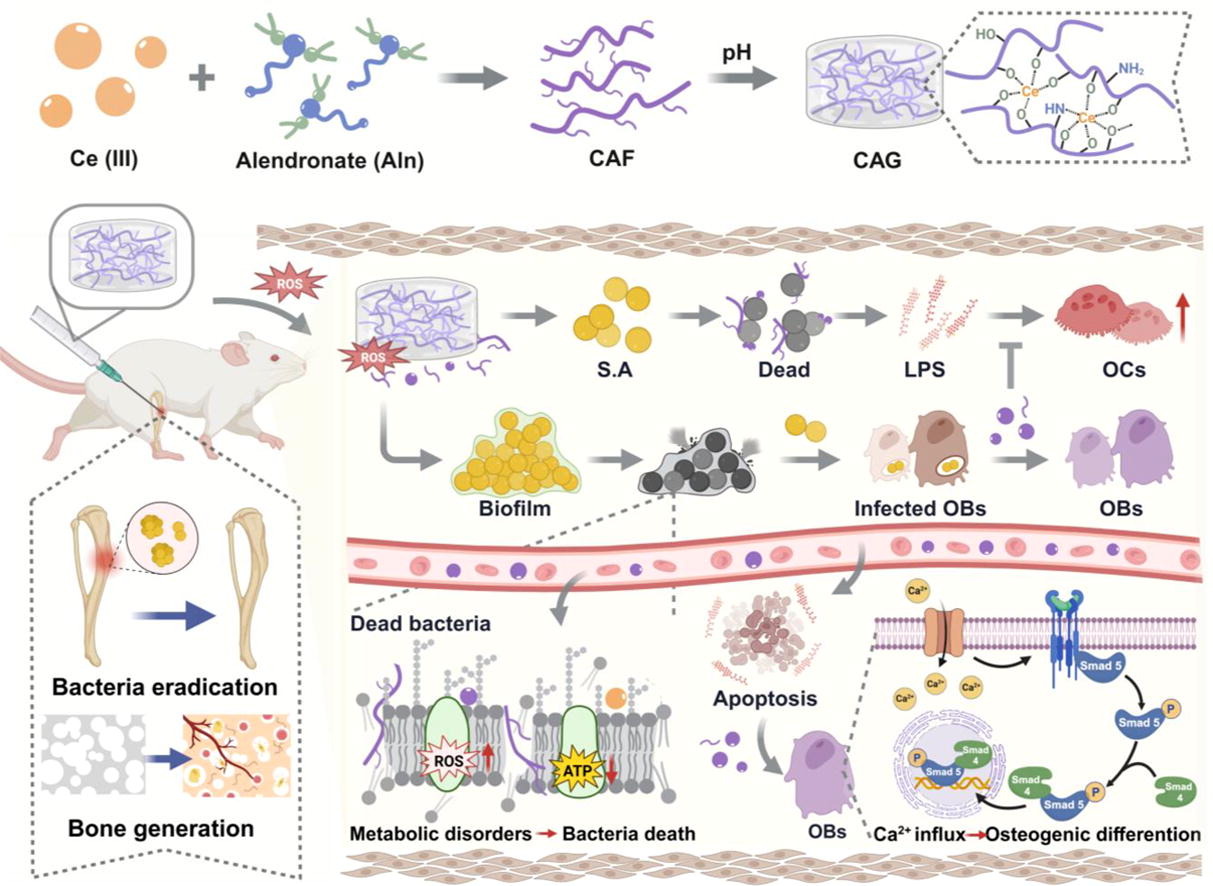
随着骨髓炎发生率的增加以及抗生素滥用导致耐药性细菌的出现,传统治疗面临巨大挑战。细菌增殖和细胞内感染通过形成生物膜,导致反复和长期的感染。同时,细菌感染引发的免疫反应破坏了骨骼的新陈代谢平衡,导致炎症性骨吸收。在此,开发了一种具有多重抗菌能力和骨代谢调节作用的铈-阿伦膦酸盐超分子水凝胶(CAG),旨在解决骨髓炎的多方面挑战。CAG水凝胶具有可注射和自愈的特点,在反应性氧种(ROS)微环境下表现出对金黄色葡萄球菌(S.A)和大肠杆菌(EcN)的显著抗菌活性,有效破坏生物膜并消除细胞内感染。CAG中的Ce离子通过破坏细菌膜和干扰细菌膜电位,抑制细菌的能量产生。此外,CAG成功逆转了内毒素引起的凋亡和成骨细胞的异常分化。RNA测序结果显示,CAG通过促进钙离子流入,调节钙信号通路和TGFβ通路,上调与Bmp2/Smad5通路相关蛋白的表达,从而促进成骨分化。在体内实验中,CAG成功治疗了由金黄色葡萄球菌引起的骨髓炎,并在7天和28天的骨髓炎小鼠模型中改善了骨组织生成。总体而言,本研究提出了一种综合疗法,旨在针对整个阶段的细菌感染并恢复骨代谢平衡,提供了一种创新的骨感染治疗方法。
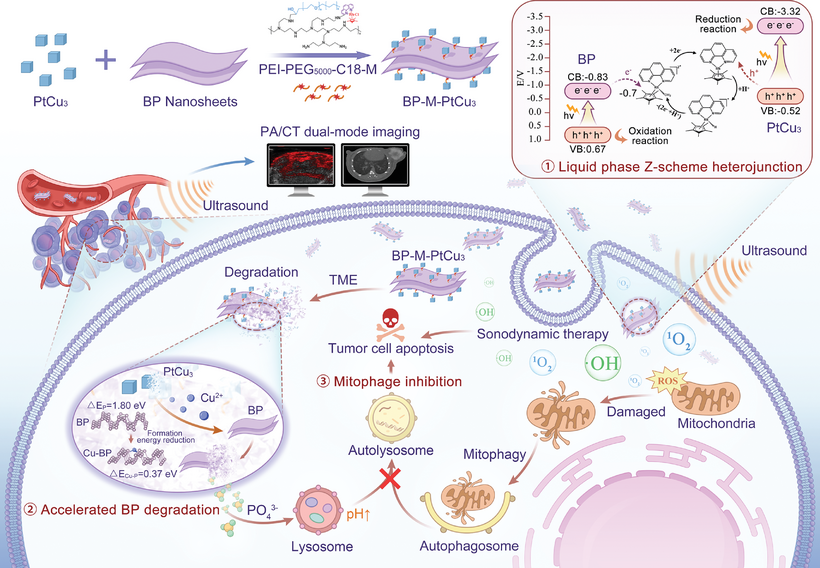
声动力治疗(SDT)作为一种有效的治疗手段,能够在肿瘤内产生有毒的反应性氧物种(ROS),用于对抗难治性三阴性乳腺癌(TNBC)。然而,由于癌细胞通过线粒体自噬机制减少线粒体氧化损伤,其治疗效果受到限制。本文报告了一种“全能”肿瘤治疗策略,将纳米声敏剂增强的非侵入性SDT与自噬抑制相结合。该策略通过合理构建声激活液体Z型异质结实现,该异质结通过两种声敏剂PtCu3纳米笼和抑制自噬的BP纳米片,通过亲水性有机连接物(PEI-PEG5000-C18)连接。共轭的电子介体(M,Cp*Rh(phen)Cl)被战略性地放置在两个声敏剂之间,以促进电子转移。基于M的Z型异质结结构延长了声激活电子-空穴对的分离时间,在超声刺激下实现高效的ROS生成。更重要的是,PtCu3释放的Cu2+通过减少磷空位形成能,加速BP降解,改善BP-M-PtCu3的生物降解性,并促进磷酸根离子的生成。这些离子提升了溶酶体pH值,抑制了受损线粒体在自噬溶酶体中的水解,从而防止癌细胞在氧化应激下自我保护,并有效消除TNBC。相信基于M的声激活Z型异质结将成为一种有前景的声敏剂结构,而声动力性自噬抑制策略为癌症治疗提供了宝贵的前景。
维持创伤的热环境对于促进组织修复和再生至关重要。然而,作为一种热疗再生治疗的潜力仍未被充分阐明。本研究展示了一种通过简单“一步”激活过程构建的光热混合水凝胶,该水凝胶能够提供稳定的光热循环能力,激活免疫反应,加速组织氧化还原和免疫稳态的恢复,最终促进创伤愈合。研究结果表明,光热HGBM水凝胶在受损创伤愈合模型中的应用,显著提高了活性氧(ROS)水平,增强了免疫反应,促进了巨噬细胞极化(M2/M1),从而诱导了促再生反应。RNA测序数据表明,45°C的温和热疗法增强了免疫反应和呼吸爆发过程,从而调节了受损组织中的免疫微环境。此外,这一过程使创伤的炎症状态向抗炎和促愈合状态过渡,这一转变由白介素-10和白介素-4等因子的产生所促进。因此,本研究提供了一种有效的热疗再生治疗策略,适用于皮肤创伤修复和组织再生。
在神经外科手术中,脑脊液渗漏是一种常见的并发症。使用贴片材料重建颅底缺损可以降低脑脊液渗漏的风险,脑脊液渗漏可能导致严重的问题,例如感染、脑膜炎、蛛网膜炎和伤口愈合延迟。理想的颅底重建材料不仅应作为防漏屏障,还应促进颅底骨再生。为了应对这一挑战,本研究设计并制造了一种 Janus 正交双层纳米纤维膜 (OPCL/PG-PCPP)。以排列的 PCL (APCL) 纳米纤维为顶层以抵抗脑脊液泄漏,而以多磷酸钙包裹的聚多巴胺纳米颗粒 (CPP@PDA,标记为 PCPP) 的垂直 PCL/明胶 (APG) 纤维设计为底层 (APG-PCPP),以促进成骨细胞迁移和成骨分化。其中,APG-1%PCPP 纳米纤维在骨髓间充质干细胞 (rBMSC) 中显示出最有效的成骨分化诱导。随后的体内动物实验显示,APG-1%PCPP 组的骨表面积 (BS) 、骨体积分数 (BV/TV) 和小梁数 (Tb.N) 是对照组的两倍,证实了良好的成骨潜力。因此,由于其独特的防漏和骨诱导特性,OPCL/PG-PCPP 膜有望成为神经外科领域适用的颅底重建材料。
口服纳米药物为癌症免疫治疗提供了一条理想的途径,但其疗效受到胃肠吸收挑战、肿瘤生理病理屏障和免疫逃逸机制的限制。在本研究中,我们提出了一种新策略,将口服跨细胞运输的多柔比星(DOX)纳米药物与组蛋白去甲基化酶抑制剂5-羧基-8-羟基喹啉(IOX1)结合,从而实现协同化疗免疫治疗。我们证明,IOX1显著增强了DOX负载的聚(2-(N-氧化-N,N-二乙氨基)乙基甲基丙烯酸酯)-聚(ε-己内酯)纳米胶束(OPDOX)的跨细胞运输能力,促进其通过不同细胞屏障(绒毛上皮、内皮和肿瘤细胞)的运输,从而改善口服吸收、血管外渗透和肿瘤渗透。此外,IOX1能够敏感化化疗,增强DOX诱导的免疫原性细胞死亡,并下调程序性细胞死亡配体1(PD-L1),破坏免疫检查点机制,协同增强强效的抗肿瘤免疫反应。因此,口服给药的OPDOX与IOX1联合使用能够有效抑制CT26肿瘤生长,展示了增强口服纳米药物在癌症化疗免疫治疗中的疗效的巨大潜力。
慢性萎缩性胃炎(AG)主要由幽门螺杆菌感染引起,随着科雷亚级联反应可能进展为胃癌。目前的治疗方案是根除幽门螺杆菌,但缺乏证据表明这种治疗对 AG 后期尤其是胃腺萎缩有效。本研究利用 AG 小鼠模型、患者样本、胃类器官和谱系追踪,揭示了胃干细胞 (GSC) 缺陷是小鼠和人类 AG 的关键致病因素。此外,从一种中药中分离出一种天然肽,可在实验性 AG 模型中激活 GSC 使胃上皮再生,并使源自患者的萎缩胃类器官恢复活力。进一步表明,该肽通过稳定 EGF-EGFR 复合物并特异性激活下游 ERK 和 Stat1 信号传导来发挥其功能。总的来说,这些发现促进了对 AG 发病机制的理解,并为 AG 治疗开辟了新途径。
少突胶质细胞对 CNS 髓鞘的形成至关重要,并且与早产脑损伤 (PBI) 和多发性硬化症 (MS) 有关,这两种疾病都缺乏有效的治疗方法。我们提出了一种药物基因组学方法,该方法鉴定具有强大的促少突胶原活性的化合物,通过评分策略 (OligoScore) 选择,该方法基于它们对少突胶原生成和(再)髓鞘形成相关转录程序的调节。通过体外神经和少突胶质细胞祖细胞 (OPC) 培养、离体小脑外植体以及 PBI 和 MS 的体内小鼠模型,我们确定了 FDA 批准的亚叶酸和动态克隆素是有前途的候选者。在模拟 PBI 的新生慢性缺氧小鼠模型中,两种化合物都促进神经祖细胞增殖和少突胶质细胞命运的获得,亚叶酸进一步增强分化。在局灶性去髓鞘/髓鞘再生的成人 MS 模型中,它们通过促进 OPC 分化来改善病变修复,同时保留 OPC 池。此外,它们将小胶质细胞从促炎转变为促再生特征,并增强髓鞘碎片的清除。这些发现支持将亚叶酸和dyclonine重新用于针对髓鞘疾病的临床试验,为PBI和MS提供了潜在的治疗途径。
牙周骨缺损是与活性氧 (ROS) 相关的牙周炎的不可逆后果。然而,不加选择地去除 ROS 被证明对组织修复适得其反,不足以解决现有的骨缺损。在牙周炎的治疗中,合理缓解局部 ROS 同时促进骨再生至关重要。在这项研究中,Zr 基大孔分层介孔金属有机框架 (MOF) 纳米颗粒 (NPs) HMUiO-66-NH2 被成功提出作为牙周炎治疗中骨再生和 ROS 清除的双功能纳米材料。HMUiO-66-NH2 NPs 在体外和体内均表现出出色的生物相容性。值得注意的是,这些 NPs 在正常和高 ROS 条件下增强了骨间充质干细胞 (BMSC) 的成骨分化,上调了成骨基因表达并减轻了氧化应激。此外,体内成像显示牙周组织中 HMUiO-66-NH2 NPs 逐渐降解。局部注射 HMUiO-66-NH2 可有效降低牙周炎诱导的 C57BL/6 小鼠的骨缺损和 ROS 水平。RNA 测序强调差异表达基因 (DEG) 主要参与骨组织发育,Wnt 和 TGF-β 信号通路显著上调。总之,HMUiO-66-NH2 在缓解氧化应激和促进骨修复方面表现出双重功能,使其成为氧化应激相关牙周炎中对抗骨吸收的有效策略。
骨缺损是临床上常见的骨科疾病。该领域的趋势是开发具有适当设计组件和结构的组织工程支架,用于骨骼修复。在此,受骨基质的有机和无机成分以及自然生物矿化机制的启发,通过微流体 3D 打印开发了一种用于骨骼修复的MgSiO3@Fe3O4纳米颗粒复合聚己内酯 (PCL) 杂化矿化支架。在 PCL 支架内掺入 MgSiO3@Fe3O4 可有效提高生物活性。此外,在支架表面制备了仿生矿化层,赋予其独特的微观结构特性,增强了细胞粘附和成骨活性,从而提高了骨修复性能。由于这些优点,体内和体外实验都表明,所设计的支架具有出色的生物相容性和骨修复性能。这些特征表明,有机-无机生物矿化混合支架可以成为临床骨修复的潜在骨移植替代品。
多重耐药 (MDR) 细菌感染已成为全球公共卫生面临的最大威胁之一。治疗困难的一个原因是缺乏适当的递送策略进入 MDR 细菌生物膜,其中厚的细胞外聚合物物质 (EPS) 层阻碍了抗生素和纳米颗粒的渗透。在这里,我们提出了一种载药脂质体和噬菌体的新型生物活性纳米偶联物,用于靶向根除骨科感染中的 MDR 生物膜。噬菌体 Sb-1 具有降解 EPS 的能力,与载有抗生素的脂质体偶联。遇到生物膜后,噬菌体 Sb-1 降解 EPS 结构,从而增加细菌对抗生素的敏感性,并允许抗生素深入生物膜。结果,使用低剂量抗生素可以有效去除 MDR 细菌生物膜,这在本研究中通过体外和体内研究得到了证明。值得注意的是,在大鼠人工关节感染 (PJI) 模型中,我们发现脂质体-噬菌体纳米偶联物可以有效降低感染区域的细菌载量,并显着促进骨髓炎的恢复。因此,人们相信噬菌体和脂质体的结合可以为治疗骨科感染开辟新的可能性,可能是深层组织中的其他感染。
