
肠道菌群参与了结肠癌的发生发展,一些致病菌如脓杆菌可以促进肿瘤的生长和转移。肿瘤为致病菌提供生存环境,形成病原体-肿瘤共生关系。破坏这种共生关系可能是肿瘤治疗的新靶点。
牙周炎是一种世界范围内流行的慢性炎症性疾病,由牙周病原菌引发,导致牙周组织,特别是牙槽骨的进行性破坏。为了有效解决牙周炎,本研究提出了一种称为 CuS@MSN-SCS 的纳米制剂。该配方包括用介孔二氧化硅 (MSN) 涂覆柠檬酸盐接枝的硫化铜 (CuS) 纳米颗粒,然后通过静电相互作用使用氨基和硫酸化壳聚糖 (SCS) 进行表面改性。该配方的目的是通过诱导 Cu 2+离子介导的 ROS 信号通路来实现有效的细菌去除。此外,它的目的是通过 Cu 2+诱导的促血管生成和 SCS 介导的骨再生来促进牙槽骨再生。正如预期的那样,通过调节表面电荷,柠檬酸钠封端的带负电的 CuS 纳米颗粒成功地被 MSN 包覆,随后使用 (3-氨基丙基)三乙氧基硅烷引入胺基,然后通过静电相互作用引入 SCS,从而产生CuS@MSN-SCS 的形成。经验证,所开发的纳米制剂不仅在体外显著加剧具核梭杆菌的氧化应激,从而抑制细菌生长和生物膜形成,而且在体内大鼠牙周炎模型中有效减轻炎症反应并促进牙槽骨再生,且没有明显的生物毒性。这些发现有助于牙周炎的治疗效果。总体而言,这项研究成功开发了一种用于对抗细菌和促进牙槽骨再生的纳米制剂,展示了临床治疗牙周炎的巨大潜力。

拔牙后,牙槽骨不均匀吸收导致软组织塌陷,阻碍了完全再生。骨质流失使得进行牙科植入和修复更加困难。受骨骼生物结构的启发,设计了一种可变形的SIS/HA(小肠粘膜下层/羟基磷灰石)复合水凝胶同轴支架来维持牙槽中的骨量。SIS/HA支架含有GL13K作为外层,模拟致密骨,而载有骨髓间充质干细胞来源外泌体(BMSCs-Exos)的SIS水凝胶作为支架的内核,类似于骨骼中的软组织。该同轴支架表现出0.82 MPa的弹性模量,使其能够自适应填充拔牙窝并维持成骨空间。同时,该复合支架富含BMSCs-Exos的内层促进了人脐静脉内皮细胞(HUVECs)和BMSCs向支架内部的增殖和迁移(约为对照组的3倍),上调了与成骨(BMP2、ALP、RUNX2和OPN)和血管生成(HIF-1α和VEGF)相关的基因表达。这诱导了支架内新血管和骨生长,解决了缺陷中心骨形成率低的问题。GL13K在前三天释放了约40.87±4.37%,发挥局部抗菌作用,进一步促进周边区域的血管化和新骨形成。该设计旨在通过同轴支架的内外双重机制在拔牙窝中实现全方位和高效的骨修复效果。
IV 型菌毛 (T4P) 是病原菌中普遍存在的聚合表面结构,使其成为有效疫苗的理想靶标。然而,细菌已经进化出有效的策略来逃避 IV 型菌毛定向抗体反应。脑膜炎奈瑟菌是典型的 IV 型菌毛表达革兰氏阴性细菌,可导致危及生命的败血症和脑膜炎。该物种进化出了几种遗传策略来修饰其 IV 型菌毛表面,改变菌毛蛋白亚基氨基酸序列、糖基化和磷酸化的性质,但这些修饰如何在结构水平上影响抗体结合仍不清楚。在这里,为了探索这个问题,我们确定了不同序列类型的菌毛的冷冻电子显微镜(cryo-EM)结构,其分辨率足够高,可以可视化翻译后修饰。然后,我们生成针对 IV 型菌毛的纳米抗体,其在体外和体内改变菌毛功能。Cyro-EM 与纳米抗体-菌毛复合物的分子动力学模拟相结合,揭示了不同类型的菌毛表面修饰如何改变纳米抗体结合。我们的研究结果揭示了细菌为避免抗体结合而使用的不同策略之间令人印象深刻的互补性。重要的是,我们还表明结构信息可用于对纳米抗体进行知情修改,作为这些免疫逃避机制的对策。
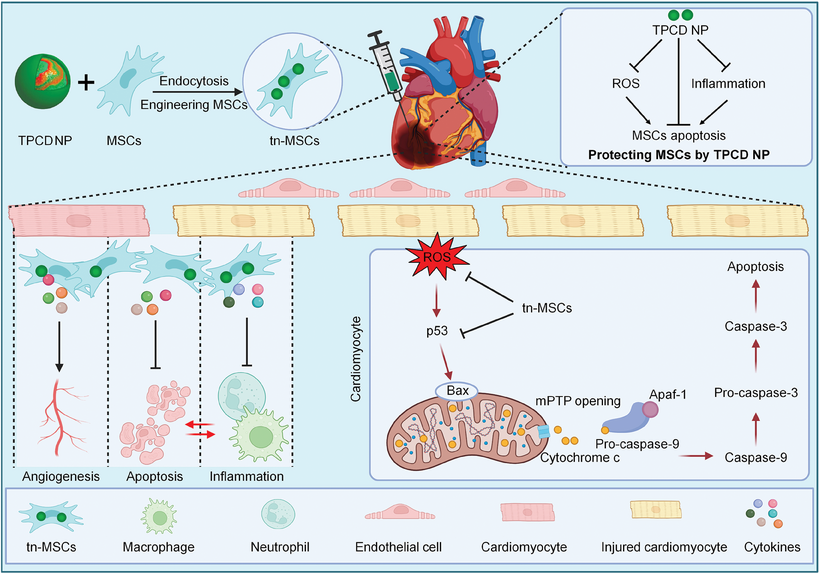
心肌梗死是冠状动脉疾病最严重的表现形式,是全球主要死亡原因之一。本研究报道了一种新型纳米治疗工程化方法,用于增强间充质干细胞(MSCs)对心肌缺血再灌注(MI/R)损伤的治疗效果。首先制备了一种抗氧化和抗炎症的纳米治疗剂(TPCD NP)。通过内吞作用成功将MSCs与TPCD NP工程化,且TPCD NP工程化不影响MSCs的干细胞特性。TPCD NP内化的MSCs(tn-MSCs)对活性氧簇(ROS)诱导的氧化应激、细胞毒性和凋亡具有抗性。在氧化应激条件下,tn-MSCs表现出比MSCs更强的旁分泌活性。相应地,tn-MSCs能有效增强病理条件下内皮细胞的血管生成。此外,tn-MSCs通过改善线粒体膜电位和调节p53信号通路,保护心肌细胞免受ROS诱导的细胞毒性和凋亡。在MI/R损伤小鼠中,与原始MSCs相比,tn-MSCs在受损心脏中的存活时间延长。相应地,tn-MSCs更显著地减少了梗死面积,改善了心脏功能,促进了MI/R损伤小鼠的心脏重塑。机制上,tn-MSCs通过减轻氧化应激和炎症、抑制心肌细胞凋亡及促进心脏修复来缓解MI/R损伤。因此,tn-MSCs有望用于治疗与氧化应激和炎症相关的心血管疾病。
侧向流动免疫测定 (LFIA) 在健康、环境和食品领域有大量应用,用于低成本、简单和快速的按需测试。通常,用户只需要添加样本,而无需从样本应用程序对结果进行任何其他干预。在 LFIA 中一个引人注目的挑战和持续追求是在不影响简单性和实用性的情况下提高检测灵敏度。我们报告了水溶性大分子拥挤剂的添加导致灵敏度的提高,这归因于抗体和微/纳米颗粒缀合物暴露于大分子拥挤环境中,同时通过条带的限制孔迁移-通过毛细作用力垫,促进负责分析物识别和信号生成的相互作用。化脓性链球菌与咽炎有关。为了立即证明灵敏度增强,我们直接在已在试剂和条件方面优化的市售设备上工作。在使用的 crowers 中,ficoll, Mr 400000 和 ficoll, Mr 70000 在不影响背景的情况下将信号提高了 5-10 倍。因为添加大分子拥挤剂是对其他增强灵敏度策略的补充,例如新型标记的设计和信号放大的引入,我们预计所提出的调制将扩展到具有各种报告基因和 LFIA 配置的众多分析物
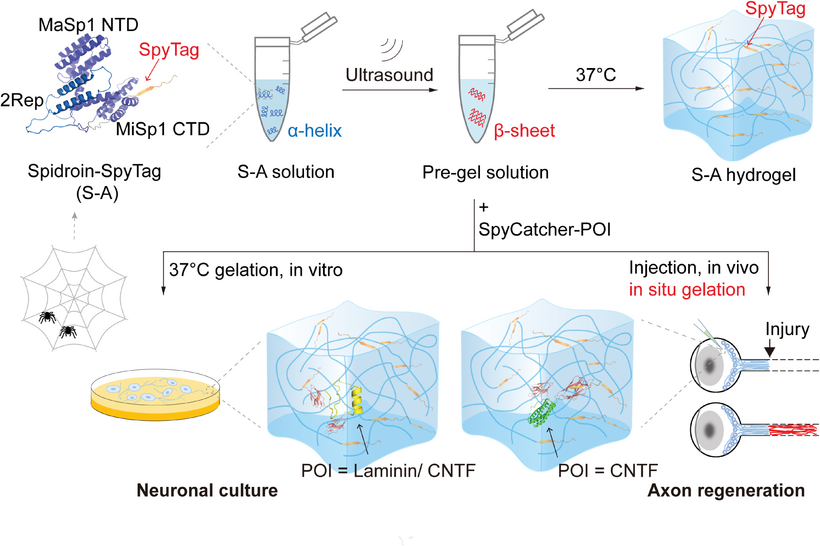
以非侵入性、安全和持续的方式递送蛋白质类治疗药物,且无需依赖病毒递送系统,这对于治疗各类慢性损伤和疾病至关重要。在众多挑战中,实现中枢神经系统损伤或疾病后的轴突再生和功能恢复,对大多数临床干预措施来说仍然难以实现,这持续推动着创新解决方案的需求。本研究开发了一种基于重组蜘蛛丝蛋白(丝素蛋白)的热响应性水凝胶系统。该蛋白质溶液经短暂超声处理后,在升高温度(37°C)时能快速发生溶胶-凝胶转变。这种热触发的凝胶化赋予了系统可注射性。利用SpyTag/SpyCatcher化学,由SpyTag融合丝素蛋白构成的水凝胶可以与各种SpyCatcher融合的生物活性基序功能化,如神经营养因子(如睫状神经营养因子)和细胞结合配体(如层粘连蛋白),使其非常适合神经元培养。更重要的是,将装饰有SpyCatcher融合CNTF的蛋白质材料玻璃体内注射到视神经损伤后的玻璃体中,可导致JAK/STAT3信号通路的持续激活、神经元存活率提高和轴突再生增强。本研究展示了一个用于神经保护和再生的可注射、持续递送蛋白质治疗药物的通用材料系统,并可能扩展应用于其他慢性疾病和损伤的治疗。
牙龈卟啉单胞菌已被证明与牙周炎的关联性最强。在宿主体内,牙龈卟啉单胞菌依赖于通过红细胞的聚集和裂解获取铁和血红素,这是牙龈卟啉单胞菌生长和毒力的重要因素。此外,获得的过量血红素沉积在牙龈卟啉单胞菌表面,保护细胞免受氧化损伤。基于牙龈卟啉单胞菌和红细胞之间相互作用的这些生物学特性,本研究开发了一种负载镓卟啉的红细胞膜纳米囊泡来模拟红细胞。纳米囊泡可以精确地靶向并粘附牙龈卟啉单胞菌,并被牙龈卟啉单胞菌裂解并作为红细胞利用。摄入的镓卟啉取代了牙龈卟啉单胞菌中的铁卟啉,导致细胞内代谢紊乱。沉积的卟啉在蓝光下产生大量活性氧(ROS),造成氧化损伤,其杀伤力通过破坏细菌代谢而增强,协同杀死牙龈卟啉单胞菌。我们的结果表明,该策略可以靶向并抑制牙龈卟啉单胞菌,减少其对上皮细胞的侵袭,并减轻牙周炎的进展。
糖尿病牙周炎中过度的氧化反应、不平衡的免疫调节和间充质干细胞功能受损,使得实现牙周组织综合再生成为一个巨大的挑战。在这里,开发了一种多酚介导的氧化还原活性海藻胶/明胶水凝胶,该水凝胶封装了导电的聚(3,4-乙烯二氧基硫氧)组装的聚多巴胺介导的丝微纤维网络和利用牛血清白蛋白纳米颗粒的硫化氢缓释系统。发现这种水凝胶可以逆转糖尿病牙周炎患者的高血糖炎症微环境并增强功能性组织再生。聚多巴胺赋予水凝胶抗氧化和抗炎活性。从牛血清白蛋白纳米颗粒中缓慢、持续地释放硫化氢,募集间充质干细胞并促进随后的血管生成和成骨。此外,聚(3,4-乙烯二氧基硫苯)组装的聚多巴胺介导的丝微纤维赋予水凝胶良好的导电性,使其能够传递内源性生物电,促进细胞排列,增加钙离子的流入。此外,硫化氢气生电偶联的协同作用通过放大牙周韧带干细胞中的自噬和通过脂质代谢调节调节巨噬细胞极化来促进骨形成。本研究为高血糖炎症微环境中电导率、活性氧清除和硫化氢对牙周组织的协同作用提供了创新见解,为气态生物电生物材料的设计提供了一种策略,以促进免疫相关疾病中的功能性组织再生。
过量饮酒和长期服用非甾体抗炎药 (NSAID) 会导致胃炎,影响全球数百万人,但安全有效的治疗选择仍然有限。虽然一系列纳米酶已被用于炎症性肠病 (IBD) 的口服治疗,但针对胃炎治疗的研究仍未得到探索。胃快速排空、剧烈的胃酸侵蚀和非食用成分构成的挑战阻碍了纳米酶在这种情况下的实际应用。在此,通过使用完全可食用的天然活性多酚、铁离子和 PVP 合成了三种类型的亚 10 nm 超小铁多酚纳米酶 (UIPNs)。UIPNs 迅速渗透胃粘膜,在胃中停留超过 12 h,并在恶劣的酸性环境中保持稳定。它们表现出优异的过氧化氢酶 (CAT) 、过氧化物酶 (POD) 和超氧化物歧化酶 (SOD) 的酶样活性。与奥美拉唑相比,所有三种类型的 UIPN 均显示出优越的活性,其中 Fis UIPN 在预防和保护酒精诱导的小鼠胃粘膜损伤方面表现出最佳性能。完全来自食物的成分,通过非共价相互作用构建成超小纳米酶,确保长期安全性,并有望在各种胃肠道疾病中发挥重要作用。
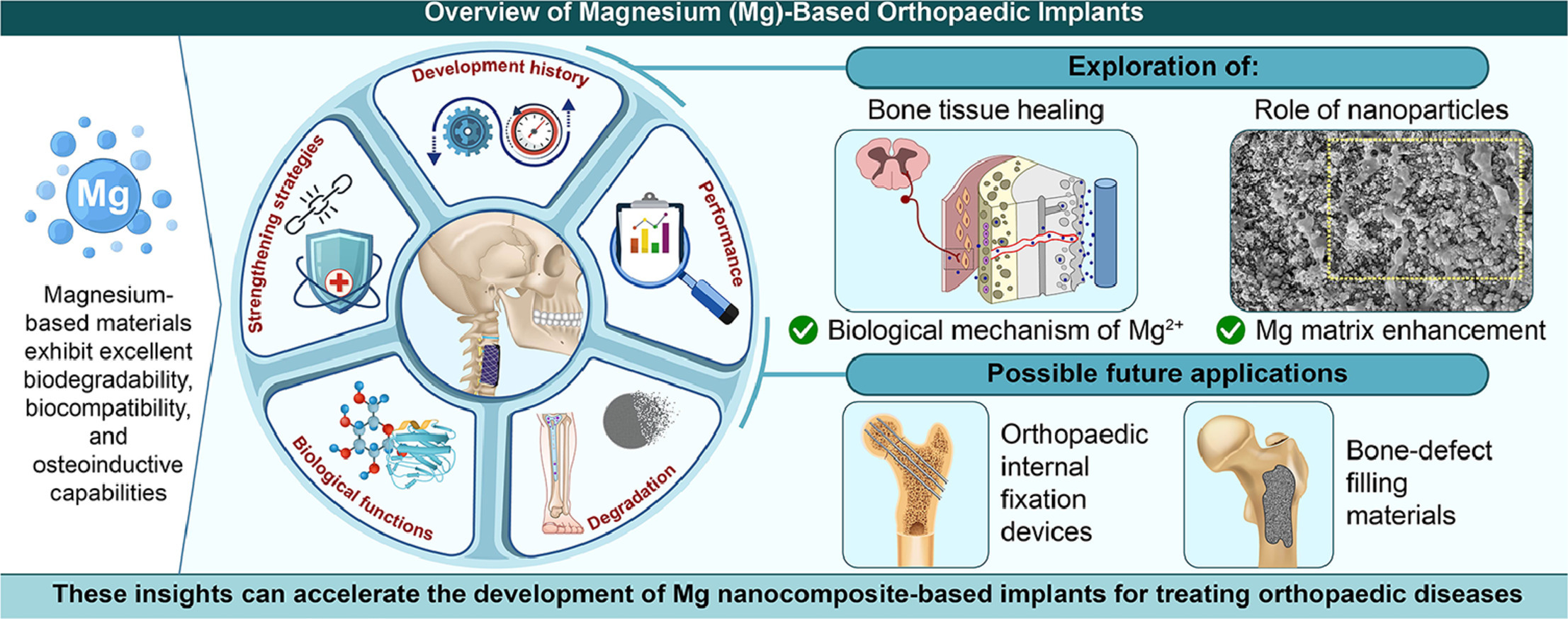
镁基材料因其良好的生物降解性、生物相容性和促进骨形成的特性,在骨科领域具有潜在的应用价值。然而,在早期应用过程中,其主要缺点是降解速率过快,这限制了其临床应用。纳米颗粒可以有效增强镁基体的机械强度和耐腐蚀性,而且可以选择不同的纳米颗粒来实现不同的生物学功能。因此,镁基纳米复合材料已经成为一类具有广泛临床应用潜力的可降解植入材料。本综述总结了镁基骨科植入物的研究进展,主要包括纳米颗粒对镁基材料的增强机制、不同纳米颗粒增强剂的作用和生物学功能、表面改性以及新制造技术的应用。此外,详细讨论了镁基材料的降解过程以及镁离子(Mg2+)在降解过程中的生物学功能。我们重点关注了Mg2+通过调节免疫微环境或多个信号通路促进骨和血管形成并抑制破骨细胞的生物学机制。最后,介绍了镁基骨科植入物的临床应用,并讨论了镁基纳米复合材料的未来研究方向。
牙龈卟啉单胞菌已被证明与牙周炎的关联性最强。在宿主体内,牙龈卟啉单胞菌依赖于通过红细胞的聚集和裂解获取铁和血红素,这是牙龈卟啉单胞菌生长和毒力的重要因素。此外,获得的过量血红素沉积在牙龈卟啉单胞菌表面,保护细胞免受氧化损伤。基于牙龈卟啉单胞菌和红细胞之间相互作用的这些生物学特性,本研究开发了一种负载镓卟啉的红细胞膜纳米囊泡来模拟红细胞。纳米囊泡可以精确地靶向并粘附牙龈卟啉单胞菌,并被牙龈卟啉单胞菌裂解并作为红细胞利用。摄入的镓卟啉取代了牙龈卟啉单胞菌中的铁卟啉,导致细胞内代谢紊乱。沉积的卟啉在蓝光下产生大量活性氧(ROS),造成氧化损伤,其杀伤力通过破坏细菌代谢而增强,协同杀死牙龈卟啉单胞菌。我们的结果表明,该策略可以靶向并抑制牙龈卟啉单胞菌,减少其对上皮细胞的侵袭,并减轻牙周炎的进展。

 苏公网安备32059002005573 苏ICP备2020067807号-1
苏公网安备32059002005573 苏ICP备2020067807号-1