Nano Lett:设计具有免疫亲和力的树枝状聚合物捕获肿瘤来源外泌体

癌症诊断和预后的新技术将推动精准医学的实践。液体活组织检查被认为是这样一项技术,因为它们是微创的,而且经常可以通过简单的抽血进行。这些测试旨在检测肿瘤定期进入血液的生物标记物,如游离DNA(cfDNA)、循环肿瘤细胞(CTCs)或包括外泌体在内的细胞外小泡(EVs)。尽管在生物标记物中CTCs可以获得最多的信息,但是这些细胞在表型上是非常罕见和异质性的,这使得临床上有意义的检测和分析变得十分困难。相比之下,cfDNA由于其含量丰富,在血液中相对容易被检测到,然而,它不能提供关于基因表达变化的动态信息。外泌体在大小、丰度和潜在的诊断信息方面位于这两个更具探索性的生物标记物之间,代表了在血液中发现的一类新兴的癌症生物标记物。这些纳米尺度的囊泡含有包装在膜中的功能性mRNA,膜上带有与它们起源的细胞相同的特征表面标记。此外,现有的文献已经将外泌体的组成和释放率与恶性肿瘤和转移联系起来,表明这些囊泡作为预后生物标志物的巨大潜力。
目前从血液中分离外泌体的金标准技术是超速离心,这是一种缓慢、难于使用且非特异性的技术。其他商业上可用的方法包括沉淀和基于尺寸的过滤技术,如ExoQuick和Exospin。然而,这些方法中的每一种都缺乏对肿瘤来源的外泌体的特异性。相反,基于免疫亲和力的方法除了具有高灵敏度和更好的样本保存性外,还可以提供这种选择性。免疫亲和技术使用外泌体或癌症靶向抗体,通常位于磁珠的表面或进入微流控通道。然而,这些基于免疫亲和力的方法完全依赖捕获抗体的结合亲和力,由于其灵敏度和特异性不足,尚未产生重大的临床影响。作者通过多价免疫识别介导结合亲和力的纳米结构聚合物表面可以显著提高外泌体免疫亲和装置的灵敏度和特异性。作者之前报道的CTCs液体活组织检查装置部分是基于涂覆了聚酰胺胺(PAMAM)树枝状大分子的表面,这种树枝状大分子有效地介导了多价结合效应,从而提高了CTCs的捕获效率。这些灵活的、超支化的纳米颗粒以两种方式促进多价捕获:高密度的官能团允许多个抗体附着到每个~9 nm树枝状大分子上;以及结构足够变形,以适应结合结构域的重定向。然而,外泌体的直径是CTCs的1/100。较小的尺寸需要开发一种新的捕获表面,以实现这种纳米尺度下基于多价结合的捕获。
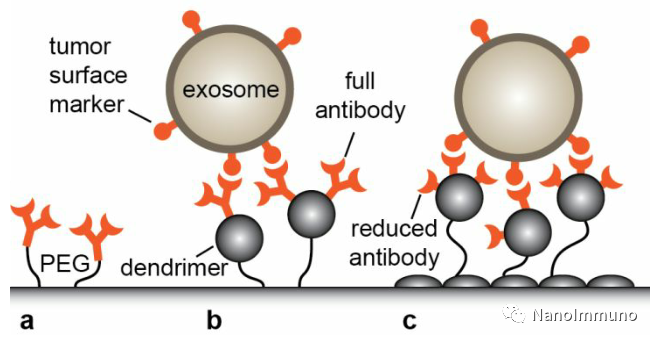
5月14日,Nano Letters在线发表了来自威斯康辛大学麦迪逊分校的Seungpyo Hong团队设计的一种外泌体捕获表面包含三层聚合物,旨在最大限度地减少非特异性结合,同时提供多价性和高度的抗体定位灵活性。首先,用部分羧化的第7代PAMAM树枝状大分子涂覆环氧官能化玻璃片。然后,将聚乙二醇(PEG)的混合物偶联到树枝状大分子和任何剩余的环氧化物基团上。聚乙二醇混合物由分子量为5 kDa和20 kDa的异双功能聚乙二醇(PEG)与另一层树枝状大分子偶联,并且用2 kDa的甲氧基-聚乙二醇(MPEG)阻断非特异性吸附。最后,将第二层羧化的PAMAM树枝状大分子覆盖在系绳上,形成两层树枝状大分子表面。下图展示了a、单独的PEG系链;b、作者之前捕获CTCs(单层树状分子)的表面和;c、这里描述的双层树状分子表面。
结果显示,纳米结构的双层树枝状大分子的表面构型通过多价结合效应实现了对外泌体显著增强的捕获。与作者之前的CTCs捕获表面相比,这项研究表明,第二层树枝状大分子在纳米尺度上显著提高了结合亲和力,使其能够高效地从细胞培养液和HNSCC患者的血液样本中捕获肿瘤外泌体,作者还通过使用原子力显微镜(AFM)定量测量了这种结合力。虽然这种捕获表面还需要进一步的开发和优化才能在临床上使用,但结果表明,树枝状大分子表面通过利用强大的结合亲和力,可以极大地提高对血浆中外泌体和其他纳米级生物标志物的检测。液体活检生物标志物的成功开发最终将为实现精确医学做出贡献。
| 温馨提示:网站部分素材源自网络,仅供学术交流勿做其他用途,如有侵权请联系我们立即删除。苏州北科纳米供应产品仅用于科研,不能用于人体,不同批次产品规格性能有差异。 |
下一篇: 纳米医学产品1


 苏公网安备32059002005573 苏ICP备2020067807号-1
苏公网安备32059002005573 苏ICP备2020067807号-1 