AFM:用于骨再生的自愈丝素水凝胶:动态金属配体自组装方法


一、文章概述
尽管丝素蛋白(SF)水凝胶的开发取得了进展,但目前用于SF凝胶化的方法具有明显的局限性,例如缺乏可逆交联、使用非生理条件以及难以控制凝胶化时间。本研究开发了一种基于动态金属配体配位化学的方法,以SF微纤维(mSF) 与多糖粘合剂之间的结合组装SF水凝胶。所制备的SF水凝胶表现出剪切稀化和自主自愈的特性,从而能填充不规则形状的组织缺损且不会产生凝胶碎裂。使用生物矿化方法生成磷酸钙包覆的mSF,其被粘合剂的双膦酸盐配体螯合可以实现可逆交联。此外,通过粘合剂的丙烯酰胺基团的光聚合反应可获得坚固的双交联(DC)水凝胶,该水凝胶无需提供任何额外形态发生因子便能实现体外干细胞增殖并加速颅骨临界尺寸缺陷的骨再生。综上,本研究开发的自修复和可光聚合SF水凝胶具有可注射性和适合形状成型的优点,在骨再生应用中具有巨大的潜力。
二、图文导读
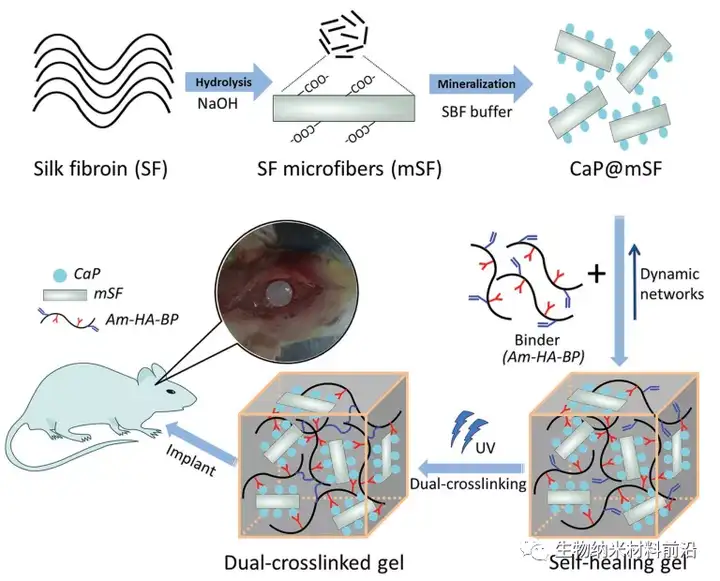
图1.用于骨再生的自修复 SF 基水凝胶的制备示意图。
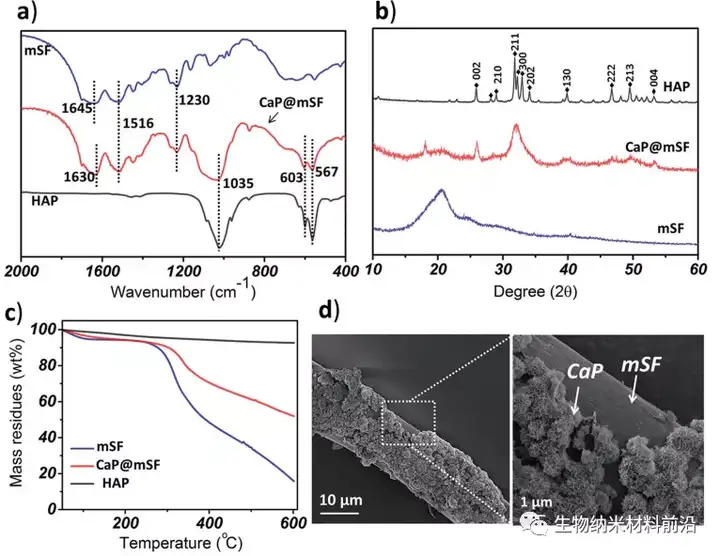
图2. CaP@mSF 的表征;a) FTIR 分析,b) XRD 分析,c) CaP@mSF的TGA曲线。
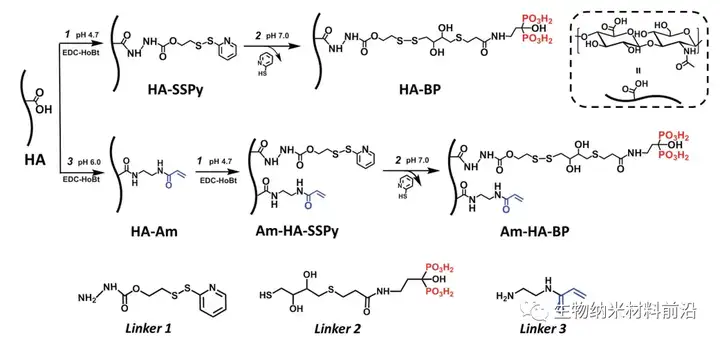
图3.基于透明质酸 (HA) 的生物聚合物粘合剂的合成。
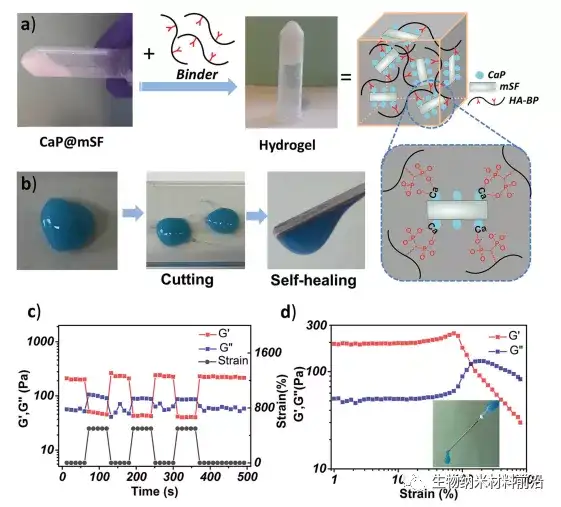
图4. HA-BP・CaP@mSF水凝胶的制备及其自修复性能;a)CaP@mSF分散体和SF基水凝胶的图像;b) 水凝胶切割成碎片和将切割碎片连接在一起后的图像;c)水凝胶在交替剪切应变变形下的储能模量;d)剪切应变过程中由凝胶向液体的转变。
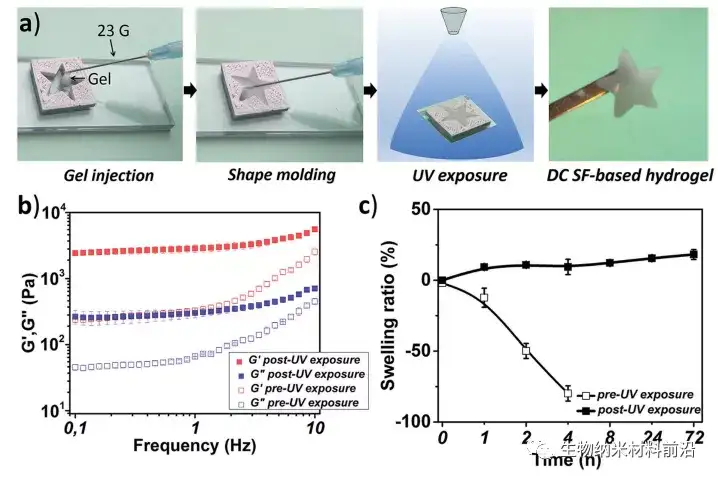
图5 a) 五星形模具中形成的Am-HA-BP・CaP@mSF 水凝胶;b) Am-HA-BP・CaP@mSF 水凝胶二次光交联前后的力学性能比较;c) SF 基水凝胶在光交联前后的溶胀。
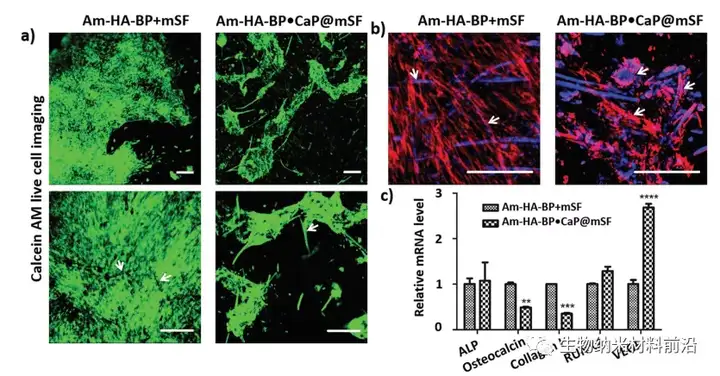
图6 .DC Am-HA-BP・CaP@mSF和Am-HA-BP+mSF水凝胶表面hMSCs的形态和相关成骨基因表达;a) 在第14天使用钙黄绿素AM进行活细胞成像;b)在第14天使用环肽-TRITC(红色)和Hoechst(蓝色)对细胞进行荧光染色;c) 第14天hMSCs 在水凝胶上的成骨标志物和生长因子VEGF的相对基因表达。
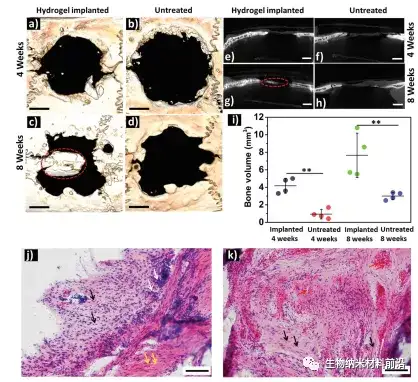
图7. DC AM-HA-BP・CaP@mSF水凝胶植入大鼠颅骨严重缺损模型后新骨形成。
三、全文总结
本研究通过态金属配体配位化学实现了具有剪切稀化和自主自愈特性的SF水凝胶的原位组装。为了完成SF水凝胶的模块化组装,本研究使用“自上而下”的方法制备了200 μm 长和10 μm 直径的 mSF,并在温和的生物矿化条件下用 CaP颗粒包被,从而产生了CaP@mSF。这些矿化的mSF与双膦酸盐修饰的 HA-BP 结合而固定在混合水凝胶网络中。由于粘合剂上的BP基团与 CaP@mSF 表面上的Ca2+离子之间的配位相互作用,HA-BP 充当了 CaP@mSF 的天然聚合物粘合剂。这些相互作用的可逆特性赋予所得混合水凝胶剪切稀化和自愈特性。这种条件允许材料成型并且不会从预期的植入部位移位以及在注射时损坏水凝胶。此外,本研究设计了具有BP和可聚合丙烯酰胺(Am)基团双重功能化的HA粘合剂(即 Am-HA-BP),并将相应的 Am-HA-BP・CaP@mSF 复合材料成型后暴露在紫外线下形成DC Am-HA-BP・CaP@mSF 水凝胶,该水凝胶具有十倍增强的储能模量。将 DC Am-HA-BP・CaP@mSF 水凝胶植入大鼠的颅骨缺损处,可在不添加任何生长因子的情况下诱导体内骨再生。这些发现意味着开发的自愈合和可光聚合的SF基水凝胶是一种很有前途的骨再生可注射支架,能够填充不规则形状的骨缺损。
文章链接:
DOI: 10.1002/adfm.20170059
本信息源自互联网仅供学术交流 ,如有侵权请联系我们立即删除。
| 温馨提示:网站部分素材源自网络,仅供学术交流勿做其他用途,如有侵权请联系我们立即删除。苏州北科纳米供应产品仅用于科研,不能用于人体,不同批次产品规格性能有差异。 |
下一篇: 纳米医学产品1


 苏公网安备32059002005573 苏ICP备2020067807号-1
苏公网安备32059002005573 苏ICP备2020067807号-1 